本文由:CIAPH根据天津瑞奇外科器械有限公司副总裁冯太川在”第七届中国医药健康行业信息化高峰论坛“演讲整理
前言:打击医药贿赂一直是医药行业的治理重点。去贿赂化的生态环境下,不仅有直接监管,还有间接影响政策。不管是“两票制”、“4+7带量采购”,行业内能够明显感觉到国家对于反商业贿赂的治理是越来越强。包括近期不少医药企业在IPO的过程中因为销售费用过高以及商业贿赂问题等被否,都反映出一个趋势,即合规是大势所趋,不可逆转的。
在CIAPH主办的第七届中国医药健康行业信息化高峰论坛上,天津瑞奇外科器械有限公司副总裁冯太川,从违规经营案例引出企业合规经营的理念和相关法律法规,并提出落实办法及合规治理体系,总结了合规经营中避免违背法律惩罚风险、实现内控需求的两方面重要涵义。

瑞奇医疗副总裁 冯太川
很高兴能够在CIAPH搭建的供行业同仁自由交流的平台上做分享。众所周知,制药行业是监管非常严格的行业,对合规的要求非常高,单纯的产品质量合规,是远远不够的。药企的合规要求,包括很多方面,比如技术、国内/国外的法律、个人隐私问题、数据收集等。
国内对于合规的要求就已经很严格了,而国外更加严格,2018年欧盟GDPR的出台,对合规有了更加严谨的要求。因此,对于药企来讲,如何做好合规的各方面,是比较现实和迫切的需求。今天想和大家交流的,是我在强生和瑞奇的工作经历中,积累的关于合规方面的经验和思考。
首先请大家来看下,近年比较突出的在合规各方面的典型例子:财务数据方面,国内某公司因,涉嫌信息披露违法违规被证监会立案调查;某外资企业贿赂政府官员被罚款;2000 年以来,因合规经营的累计罚款,总数超320多亿美金,著名药企全都榜上有名;对国内药企违规事实饼状图分析可知,“陈列与存储”违规问题最为突出,“文件管理”、“设施与设备”违规条例也很严重。
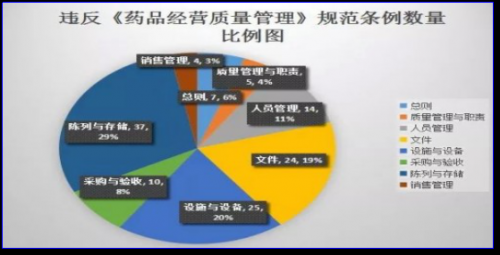
以上事例,涉及到合规问题的多个方面。那什么是合规经营?与此相关的法律有哪些?
精细化管理一:合规经营在于生产和流通
合规管理是指公司制定和执行合规管理制度,建立合规管理机制,培育合规文化,防范合规风险的行为。合规管理与业务管理、财务管理并称企业管理的三大支柱,是内控的一个重要方面 。
医药/医疗企业合规经营包括生产和流通(销售)两大环节。其中,生产环节的合规重点在于药品/医疗器械的质量问题,包括研发环节的数据核查和一致性评价、生产工艺核查、生产环保合规等。流通(销售)环节的合规主要着重于挤出药品/医疗器械价格的不合理成分,打击医药/医疗器械流通和营销的灰色环节。2018年,随着两票制在全国正式铺开,政府将加大打击医药/医疗器械流通领域的过票、洗钱等违法行为。
精细化管理二:了解合规经营的相关法律法规
在合规方面的法律法规,主要有以下:
医药医疗行业生产合规标准:《GXP》,药品研制和开发行业委员会颁布的《药品推广行为准则》,在数据准确、产品质量、追溯等方面有很严格的要求。
2018年中国新版《药品数据管理规范》、《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》等其他行业法规法则;中国刑法《反不正当竞法》、《关于禁止商业贿赂行为暂行规定》;
美国FCPA《反海外腐败法》;
2002 US SOX《美国萨班斯法案》,被称为“美国商业界影响最为深远的改革法案",使上市公司不得不考虑控制IT风险在内的各种风险,要求对财务数据不能做修改;随后日本也颁布了相应的法案(财务数据),中国在此基础上,也出台了相应法律;
经济合作发展组织(OECD)的《禁止在国际商业中贿赂外国公职人员公约》;
香港《防止贿赂条例》、《上市公司防贪指引》,英国《反贿赂法》,日本《不正当竞争防止法》,联合国反腐败公约;
EU General Data Protection Regulation GDPR (《欧盟个人隐私、个人资料法》;
美国 HIPAA (Health Insurance Portability & Accountability Act)。
以上相关的法律法规等,都在督促着医药、医疗器械生产企业朝着合规经营的道路深入前进。
精细化管理三:落实合规经营
药品/医疗器械生产企业怎样才能有效落实合规经营呢?以下几个方面是必不可少的:
必须建立完善的合规治理体系/结构;财务风险管理/审核体系;信息安全( 数据) 文件/文档管理体系;员工培训规划/系统。
必须承担主体责任,对产品全生命周期的安全性和有效性负全部责任;承担不良反应/医疗事故直报和对药品/器械质量持续提升的任务,以更高质量的产品和服务来保障患者的安全和健康 。
严格把控质量流程管理、优化培训体系,建立“记录和档案”管理体系并配备全生命周期的GMP文件管理方案,是保证医药/医疗器械企业合规经营的重要事项。
需要指出的是,想要落实药企经营合规,仅从IT的角度出发,是很难落地的。一方面,这里涉及财务的风险管理问题,虽然可以通过IT设备或系统的手段去避免,但并不能杜绝;另一方面,需要保留产品质量的文件凭证,这又引出了另外一个体系,即文件管理体系。所以,这不是单靠系统或是IT人员就可以推动的,需要集团由上到下的实施。
合规经营治理体系包括以下内容:
合规治理结构,高层态度明确,并由上而下的全面推动;明确各级管理层和员工在合规体系的角色与责任;
合规风险评估,加强内审,识别公司运营各层面存在腐败风险,制定弥补方案;
制定一整套书面的和规政策、制度、流程和标准,防止贿赂、贪污等腐败风险;
培训,董事会和管理高层定期向员工传达合规经营的决心和要求,并要求管理层和所有员工签署合规经营声明(每年一次);
合规审计,尤其是高风险领域(市场费用支出、佣金、样品、礼品、业务招待、捐赠);
尽职调查,对代理商、经销商、供应商做背景,尽职合规调查/审计。
下面的介绍,主要以某外企的合规经营治理体系为例,其具体的条例规定非常详细,包涵以下内容:
1、Hotline / FAQ document (热线电话,含常见问题)
2、FCPA_HCBI_Module_Summary (美国防海外腐败法重要条款)
3、HCBI Escalation Procedure (内部合规经营问题升级流程)
4、HCBI Acknowledgement (合规经营声明)
5、HCP Mutual Arrangements (Compensation) (与医药医疗行业专业人员合作合同/薪酬)
6、HCP Initiated Research Grants (医药医疗行业专业人员发起科研项目拨款)
7、Managing HCBI Incidents (处理合规经营问题流程)
8、Product Training (产品培训)
9、Providing Samples (样品提供)
10、Providing Gifts (送礼政策)
11、Tender Process (政府招标流程)
12、HCP Travel and Accommodation Standards (招待医药医疗行业专业人员-差旅和食宿标准)
13、Employees Training Materials (员工培训资料)等。
落实合规经营,对于企业来讲,还需要注意相应的法律法规要求,并做到以下方面:




合规经营治理体系的重点,还包括生产质量体系/追溯系统,如(记录和档案)管理体系 RIMP、信息资产保护政策(IAPP)、关键文档/记录(Vital Records)、文件/记录保存期限(RRS)、BCP(企业灾难恢复计划)等。药企要严格把控质量流程管理 、优化培训体系、建立“记录和档案”管理体系,并配备全生命周期的GMP文件管理方案,这是保证医药/医疗器械企业合规经营的重要事项 。
从IT角度来看,要做好合规经营,就要做好以下方面:
做好系统验证(CSV)/数据备份
BCP(灾难恢复计划)
财务合规(SOX-ERP系统,配置角色和权限,职责分离,防止腐败,财务数据准确、完整、即时;AI等技术,财务机器人的预警提示分析风险)
信息安全管理(文控系统加密、备份,Mobility & Cloud(移动/云)/Block Chains (区块链)-数据安全,Big Data & Analytics(大数据分析)。






