2017年8月17日,CIAPH(中国医药健康信息化联盟)对科伦药业信息总监徐华林进行了一次群访谈。在2016年,科伦已在下属23个生产基地实施了赛默飞的LIMS实验室管理系统和BIOVIA相关系统,徐华林总监详细介绍了LIMS系统实施的背景,以及系统的选型和项目实施的具体规划。以下系CIAPH对群访内容的整理:

主持人:先请徐总做一下自我介绍。
徐华林:各位同仁,大家好,我是来自科伦药业的徐华林,有幸和大家一起探讨制药企业QC实验室信息化。科伦药业创立于1996年, 2013年科伦集团营业收入超过300亿元、利税超过20亿元人民币。根据商务部和工信部2012年医药统计年报,科伦集团旗下的商业和产业双双进入全国前十强。2010年6月3日,科伦药业在深圳证券交易所成功上市。科伦药业生产和销售包括输液、粉针、冻干粉针、小水针、片剂、胶囊剂、颗粒剂以及口服液等25个剂型共468个品种的各类药品。其中,输液领域拥有109个品种共245种规格的产品,是中国输液行业中品种最为齐全和包装形式最为完备的医药制造企业之一。
主持人:科伦集团作为具有药品研发、药包材生产、医药原药、中西制药等多领域产业发展的综合性集团,在考虑集团实施LIMS有何需求背景,本次系统实施范围是怎样的?如何进行系统的选型和项目实施规划?
徐华林:科伦在五年以前,就在考虑实施LIMS系统,当时的初衷和现在不一样,现在大家可能面临的合规要求更高,数据完整性要求是考虑的第一要素。原来的出发点比较简单,首先是要适应国家法律法规,特别是新版GMP的新要求,2011年新版GMP实施后,对检验记录、风险评估、产品回顾等提出更高的要求。举个例子,原先企业在出检验报告是可以出具多个亚批检验报告的,一个报告上可以有多个亚批的数据,工作量就可以节约一些。
2011年后,CFDA要求必须每个批号(包括每个亚批号)都必须出具单一的检验报告。所以,从原始检验记录、台账和COA报告的工作量成几十倍增长。这是当时我们考虑实施LIMS系统最重要的原因,而且科伦药业生产规模大、产品结构复杂,新版GMP 的实施导致质量部各检验室记录书写量大、产品检验数据收集难,需要投入大量的人力和物力来保障质检工作的合规性。
当然,5年前的系统实施是以提高检验效率为第一目标,实施的范围我们界定了所有生产基地的所有品种,我们考虑分步实施的策略。当时科伦提出了一个“大质量观”的理念,我们需要把全程QC检测过程管起来。
关于选型,当时也是一件比较困难的事情,因为五年前的情况和现在差异比较大。当时国内实施过的药企基本没有,所以选择面比较少,我们仅有参观和考察过的实施企业就是几个外企,包括杭州的眼力健,国内做LIMS的有药检院和各省的检验所以及石油系统的企业。科伦信息化选型和公司的其他项目选型都一样,遵循公司的一个基本制度,被称之为“三三制”,也就是至少三家解决方案,公司三个以上部门和经过三次以上谈判确定。
最后科伦药业选择了北京创腾代理的赛默飞和达索的LES,这也是经过多次对比和原型验证的,主要考量以下因素:是否解决核心问题,是否满足合规要求,性价比、实施经验如何。并且对几个重要的问题有原型验证。
主持人:您提到该项目目前已在23家生产基地导入,那么在LIMS系统实施中,不同的生产基地对于系统功能的要求是否也有差异,如何解决统一规划和分布实施在需求应有上的差异和矛盾?在四期项目实施中都遇到哪些难关令您记忆犹新?
徐华林:23家单位其实是有差异的,主要表现在产品结构不一样,实验室环境也不一样。从一开始我们就确定统一的IT架构和流程,这一点非常重要,这样我们在不同阶段实施的时候,不会再考虑部署系统的问题。我们下属的所有单位全部统一使用集团数据中心的生产系统、测试验证系统和开发系统,后面只是培训和仪器链接、验证。业务流程通过本项目实施,也全部梳理和统一,不争论,只执行。
所以我们第一期实施周期比较长,在新都基地大概花了一年半,其实主要的时间也是确定方法和流程。后面基本上每个基地只需要两到三个月,产品结构一样的,比如同样是输液基地,其实方法和静态数据(指SOP 内嵌化、COA模板电子化等)是可以复用的,工作量可以节约很多。后续几期的实施,基本上由我们自己的人就可以完整完成从培训、仪器连接到试运行、正式上线、验证的全部流程了。我们也了解到,部分省级检验院在上LIMS系统时,花了大量的时间在静态数据的准备上(静态数据指SOP内嵌化、COA模板电子化等)。
在保障基地与集团数据中心数据互联的安全性方面,我们的业务管理员是从质量部协调过来的超级管理员,基本与IT 无关,主要是将系统的权限管理、配置管理和各业务部门独立出来,符合IT内控的要求。不能将业务超级管理员放在业务部门,包括我们的财务系统、供应链和物流系统也是按照类似的管理。
传统以LIMS为主架构的缺陷:
传统方式一(纸质原始记录);
- 无法确保实验人员完全按照SOP执行检验流程;
- 无法避免数据的人工填写错误;
- 无法及时获得数据修改的情况;
- 手工方式,仍然无法解决实验室低效、重复及错误率高的状态;
- 实施风险较高;
传统方式二(原始记录电子表单):
- 仍然无法确保实验人员完全按照SOP执行检验流程;
- 无法进行SOP版本的自动更新和发布(此为本系统的关键需求);
- 电子表单和仪器连接均需要专业的开发人员,后期维护成本巨大;
- 实施风险较高,实施成本不可控;
所以第一个难点就是彻底解决大量的手工记录的问题。科伦药业产品结构比较复杂,因此在项目实施过程中,如何对大量的基础数据进行整理、维护和标准化,是一个非常巨大的挑战
在科伦新都基地项目组和创腾科技的通力配合下,对SampleManager LIMS中静态基础资料数据的维护已达2万4千余条,构建WEB实验记录模板320个;在较短时间内,利用LES的Method Build构建了SOP检测方法执行模板4447个,由于需要正式环境、测试环境和验证环境,对数据复用提出了新的要求。
感触最深的是我们科伦利用自己的力量,建立从WORD宏模板到系统模板的快速建模。现在大家如果使用BIOVIA 的Method Build也可快速建模,否则几千个模板是需要耗费大量精力。
第二个难点,采用LIMS+LES(ELN)的产品体系架构,需要对传统的Sample Manager LIMS产品进行部分升级和开发,项目组决定开发相应的WEB接口,利用浏览器模式,提供更好的便利性和易用性,节约培训成本;采用远程虚拟应用,降低用户对终端和网络的要求,提高安全性和降低实施风险。
大家知道,LIMS许可比较贵,所以我们在LIMS和LES之上加了一个WEB壳,完成样品接收和分发的管理,这个是创腾根据项目开发的,摆脱了大量用户对许可的限制,采用远程虚拟应用是满足集团部署的一种手段。刚开始,我们考虑了是思杰的解决方案,但是费用太贵,后来我们选用的是已经成熟使用的国产虚拟桌面极通,完全满足系统的要求,除新都基地外,其他都采用虚拟桌面。
大量的原始检验记录和COA报告生成,试图诸如水晶报表工具来实现具有很大困难。科伦项目组开发了专用的Word宏模版定义工具,使得关键用户可以在不需要IT技术支持下,利用现成的Word模版得以轻松完成。原始检验记录和COA报告的批量自动生成。电子签章的批处理作业,质检报告和ERP用户下载自动处理。同电子监管码、ERP系统的数据集成(主数据、请验和放行),以及特使符号及修约问题。
我认为项目做得最好的就是同ERP、电子监管码各系统的高度整合,下图是几个系统的整合图:
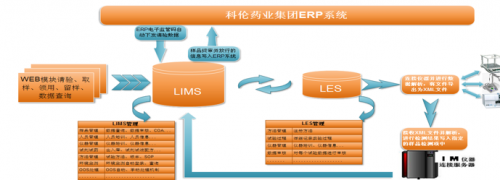
样品的请验和放行需要和电子监管码和ERP系统整合,经电子签章的COA报告自动关联ERP系统的原始发货记录,用户可以自动下载质量部的的报告(权限严格分离,必须是自己的发货记录),特殊符号和中国修约规则也是困扰当时的小问题,也都圆满的解决了。
主持人:LES和LIMS 是同步规划和实施的吗?各自的功能是什么?
徐华林:LES和LIMS 是同步规划和实施的。
LIMS主要包括样品管理模块、人员管理模块、仪器管理模块、库存管理模块、环境监测模块、OOS管理模块、稳定性管理模块、供应商管理模块。
WEB功能主要包括下发请验管理、取样确认管理、可见异物检测、试剂试液管理、台账管理以及库存信息管理。
报告、文件管理包括LES原始记录报告审核、COA报告审核、产品审核放行、仪器谱图管理以及COA报告管理。系统集成接口包括ERP信息管理接口、符码系统接口、LIMS TO ELN接口、CA电子图章接口、仪器数据传送接口。下图是大家比较关心的LES(ELN)的功能:

解释一下LES和ELN,大家把电子实验记录称之为ELN,如果实验SOP是强制标准,过程和方法是不能变化的,称之为强制执行系统既LES。在生产实验室,不同研发实验室,SOP都是国家药典规定好了,所以都是强制方法。如果大家需要在研发实验室环境下使用,就应采用ELN。
ELN同仪器仪表的连接方式:
第一种是串口/并口仪器的数据实时读取,它通过协议转换(Convertor),实时的读取串口/并口所产生的数据。它具有部署简单方便的特点。不需要专业的开发人员编写程序,仅需要简单的配置就可以读取相应的数据,后期维护也较方便。
第二种:工作站文件的解析数据溯源追踪,IDS系统支持多种文件格式的解析,在实验过程中记录相应的结果,并支持查看数据的原始文件图谱等。也就是支持单机版的文件解析。
第三:网络版CDS的数据库文件解析,这需要根据实验室设备情况来选择连接模式。现在好多药企都在对色谱等设备进行CDS改造,ELN是都可以支持的,包括所有主流的设备。当然不可避免还有没有任何接口的设备,那就只能手工录入,也系统支持批量录入。
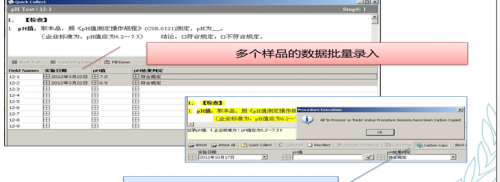
强调一下,批量导入受到数据完整性的挑战,需要在SOP流程上严格规避。下图是数据采集的界面:
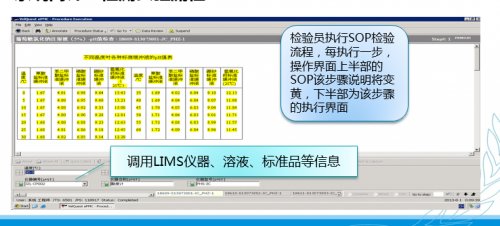
图谱的采集:
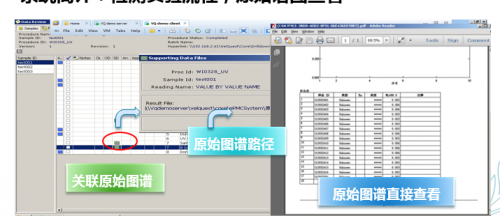
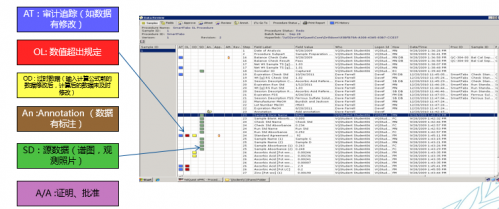
超标处理和审计追溯:
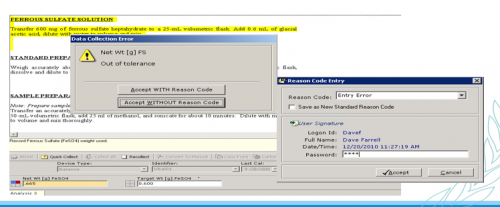
数据审核和放行:
自动生成原始检验记录和台账:

然后系统会自动生成COA报告,不光有公式和计算,还有很多特殊符号和修约规则。当然,要把Word模板变为系统的变量模板,这是项目实施的一个难点。
主持人:请问徐总,对于项目实施方的选择有哪些可以分享的经验?此次两个项目均由北京创腾实施,实施项目管理能力如何,系统上线运行后运行效果如何?
徐华林:项目经过分阶段几期的实施,应该说还是比较顺利的,在实验室信息化领域,我个人还是比较认可创腾,另外还有北京三维和北京英普思科技。科伦的项目上线后主要的效果我个人认为除了效率和无纸化显性的因素外,其实和现在要求的数据完整性刚好契合。这个过程中,我的心得是:实施比产品更重要,运维比实施更重要。
主持人:您在2017年还有哪些信息化规划和项目实施?未来3-5年企业发展战略规划对于信息化的实施有哪些工作要做?
徐华林:未来科伦的主要重点讲是生产和研发领域的信息化工作,今年我们也申报了一个国家智能制造项目。现在正在试点试探车间物流和成本的工作,还不能称之为MES,重点解决生产批记录和车间物料差错控制的问题。也就是“专注重点问题,解决核心矛盾”。
徐华林简历
四川科伦药业股份有限公司 信息总监
工业和信息化部两化融合技术指导体系委员
中国化药协会两化融合专业委员会 副理事长
成都市企业信息化促进会 副理事长
擅长于集团大型企业信息化战略规划、信息化项目管理和实施、企业IT治理体系的建设。先后主持和建立了科伦药业供应链、财务、资金、TMS、HR、WMS、LIMS、QMS、BI高清视频会议、企业协同、电子采购系统、企业竞争情报系统、灾备体系等数十个系统。科伦药业被国家工信部评定为“国家级两化融合示范企业”,本人被评为2016全国百佳CIO。
关于科伦药业
科伦药业创立于1996年, 2013年科伦集团营业收入超过300亿元、利税超过20亿元人民币。根据商务部和工信部2012年医药统计年报,科伦集团旗下的商业和产业双双进入全国前十强。2010年6月3日,科伦药业在深圳证券交易所成功上市。
科伦药业生产和销售包括输液、粉针、冻干粉针、小水针、片剂、胶囊剂、颗粒剂以及口服液等25个剂型共468个品种的各类药品。其中,输液领域拥有109个品种共245种规格的产品,是中国输液行业中品种最为齐全和包装形式最为完备的医药制造企业之一。科伦药业在输液行业和抗生素硫氰酸红霉素制造领域创造了两项世界冠军。
关于CIAPH
“中国医药健康信息化联盟”, 英文为“China IT Association of Pharm & Health Industry”,以下简称“CIAPH”。 CIAPH的成立是为了建立一个针对中国医药健康产业用户群的专业联盟,促进医药健康企业之间的自由交流和互助;分享用户最佳实践,最大化用户对IT的投资回报。CIAPH是独立的、中立的、自发的联盟,源于用户且回报于用户的组织。






